Aki passaram...
01/12/08
Pegada Ecológica em Portugal
Pegada ecológica I
 Neste momento estamos a usar energia a uma taxa superior à sua capacidade de reposição. Para isso recorremos ao "capital natural" acumulado ao longo de milhões de anos, exaurindo-o. Para que a sociedade seja sustentável, a Pegada Ecológica terá de ser inferior à capacidade de carga (ou biocapacidade) do planeta ou região.
Neste momento estamos a usar energia a uma taxa superior à sua capacidade de reposição. Para isso recorremos ao "capital natural" acumulado ao longo de milhões de anos, exaurindo-o. Para que a sociedade seja sustentável, a Pegada Ecológica terá de ser inferior à capacidade de carga (ou biocapacidade) do planeta ou região.A Pegada Ecológica permite calcular a área de terreno produtivo necessária para sustentar o nosso estilo de vida.
Nessa data, a Pegada Ecológica média mundial era 35% maior do que a capacidade de regeneração do planeta.
21/11/08
Cidades e vilas sustentáveis
Os participantes na Conferência de Lisboa, de 1996, aprovaram o documento intitulado "Da Carta à Acção".
Seguiu-se Conferência de Hanôver (2000).
19/11/08
Protocolo de Quioto... E Bali?

1. Onde e quando foi adoptada a Convenção-Quadro das Nações Unidas sobre Alterações Climáticas?
2. A UE respeitou o seu compromisso referente a essa Convenção para o ano 2000, mas outros países não o fizeram. Então, o que foi decidido depois?
3. Quando é que a UE ratificou o protocolo? E Portugal?
3.1. Quando é que ele entrou em vigor?
3.1.1. Por que motivo só aconteceu nessa data?
3.2. Quando é que a Austrália o ratificou? Em que circunstâncias?
4. Em que consiste o Protocolo?
4.1. Qual é a sua meta global?
4.2. Qual é a meta para a UE?
4.3. Qual é a meta para Portugal?
4.4. Indique duas iniciativas da Conferência de Nairobi.
4.5. Qual foi o objectivo principal da Conferência de Bali?
4.5.1. Quais as posições do Canadá, Japão e EUA em relação ao objectivo dessa conferência?
17/11/08
Cimeira da Terra, antes e depois
Procure os apontamentos enviados para o seu email, para responder da melhor forma às seguintes questões.
1.1. O que se decidiu nessa conferência em relação à Educação Ambiental?
2. Relatório de Brundtland.
2.1. Que outro nome tem esse relatório?
2.2. Em que ano foi publicado?
2.3. Quem o elaborou e quem dirigiu o grupo de trabalho?
2.4. Por que motivo foi elaborado?
2.5. Qual foi o conceito novo que trouxe para as questões ambientais?
2.6. Quais eram as metas que o relatório definia a nível internacional?
2.7. Quais são as três vertentes do Desenvolvimento Sustentável?
2.8. Defina Desenvolvimento Sustentável (DS).
3. Passadas duas décadas sobre a aceitação da ideia de DS, a ONU apresentou um relatório sobre a evolução do Ambiente, diz que nestes 20 anos depois do relatório de Brundtland quase não houve avanços e que, no essencial se mantêm os problemas ambientais mais relevantes.

05/11/08
Entrar neste ambiente

Para cada grupo iniciar a sua ligação ao "Ambientalnet" deve trabalhar duas das seguintes possibilidades:
1. Um dia temático sobre ambiente e apresentá-lo da melhor forma possível no âmbito desse projecto de sensibilização ambiental;
2. Escolher uma notícia sobre questões ambientais, comentá-la e desenvolver o tema em causa;
3. Escolher uma ONGA, apresentá-la (mesmo o contéudo do site) e divulgá-la.
29/10/08
Educação Ambiental - Evolução e História - sec XX
1. Carta de Belgrado
2. Relatório Brundtland
3. Cimeira da Terra (e Agenda 21)
4. Cimeira da Terra (e Desenvolvimento sustentável)
5. Conferência de Quioto
Tema suplementar:
Cimeira para o Desenvolvimento Sustentável (sec. XXI)

Os grupos deverão referir:
- o local, a data e duração dos encontros, os organizadores
- a preparação a que estiveram sujeitos
- as medidas e decisões tomadas
- os efeitos/resultados dessas medidas
- o envolvimento de Portugal
Aconselha-se liberdade de pesquisa mas sempre com a cuidada selecção de informação e de linguagem. Use o ECO-FIND.
Os trabalhos de grupo serão apresentados na aula.
Trabalho a desenvolver nas próximas 3 aulas (semana e meia); Seguir-se-á a apresentação.
21/10/08
Química: primeiro teste de avaliação
Manual do 9º Ano
da p. 172 à p. 224
caderno de actividades - p. 77 à p. 90 (até ao exercício 49).
Esses conteúdos repetem-se e aprofundam-se no manual do 10ºAno:
Manual do 10ºAno
da p. 12 à p. 15
p. 32 e p.35 e exercícios 1 e 2 da p. 37
p. 38 à p. 41 e exercício 1 da p. 43
p. 100 à p. 108 (sem configurações electrónicas, mas antes distribuições electrónicas)
exercício 7 da p. 109 (distribuições e não configurações)
p. 110 à p. 114
exercícios 2, 3, 4a)b), 6, 7, 8, 10, 11, 14, 15 e 16 das p. 115 a p. 117
p. 118 à p. 120
p. 194 à p. 200 e p. 203
exercícios 2, 3, 4, 5, 6 das p. 201 e 202
exercícios 3, 4, 5 e 6 da p. 206.
Não esquecer que na reprografia se encontram os objectivos de todo o módulo 1 (e seguintes) assim como a correcção da última ficha formativa.
Vamos lá a resolver já este módulo!!!
E até se podem fazer uns jogos de química e da TP, por aqui ---» FQ-sapo
23/09/08
Adopção de elemento químico

Apresentação dos trabalhos à turma: 20 -24 de Outubro.
19/09/08
Curso Profissional
17/05/08
Maratona de 7


Cada um dos 5 grupos foi colocado perante as mesmas 3 situações problemáticas. Num período de 30 minutos foram à procura de entendimento e da solução que poderia contribuir para um bónus na avaliação final. As 15 respostas são os 15 comentários do post anterior.
15/05/08
Da melhor discussão... nasce a solução

A Tatiana resolveu trazer água recolhida pelo desumidificador lá de casa para poder determinar a sua dureza. Ficou admirada quando verificou que após a adição de mais de 50 mL de EDTA (dissódico) o negro de eriocrómio-T ainda não tinha mudado de cor. Afinal parecia que o método escolhido não funcionava. Explique o que sucedeu.
Situação 2
Uma aluna do 8ºAno considera que existem poucas análises feitas à água do concelho.
Indique-lhe a classificação de diversos tipos de águas (4 exemplos de classificação) e apresente alguns dos problemas mais comuns da qualidade das águas do concelho.
Situação 3
A Patrícia analisou uma água de um tanque e o Rui determinou esses mesmos parâmetros para a água de uma fonte.
Quer o teor em cloretos, quer a concentração de oxigénio dissolvido são muito diferentes. A dureza da água era semelhante, mas reduzida.
Encontre explicações para os resultados das análises efectuadas.
Cada grupo deve responder na forma de comentário a esta mensagem.
Cada melhor resposta terá um bónus de 1,0 valores na classificação do teste.
21/04/08
Polímeros
7ki - As proteínas são polímeros naturais
7ki - Actividade com polímeros: EPS e látex
7ki - Testes a plásticos

Azoto na água
- Um dos problemas correntes associados ao azoto acontece no controlo da qualidade de água dos aquários.
- Nitratos em águas subterrâneas: Ribatejo (1996-2000).
- Método para remoção de nitratos: permuta iónica.
17/04/08
Actividade com polímeros: EPS e látex
EPS - Poliestireno Expandido
- uma introdução sobre o polímero da actividade (classificação, propriedades, aplicações, vantagens/desvantagens, possibilidades de reciclagem) e sobre cuidados (regras de segurança) a ter com os reagentes e materiais utilizados.
- uma discussão sobre as observações e uma explicação científica do que sucedeu.
Não esquecer a indicação das fontes de informação! BOM TRABALHO!
14/04/08
Testes a plásticos
- teste da densidade (em água, em álcool isopropílico e em óleo de milho)
- teste da chama (com fio de cromoníquel)
- teste da acetona
- teste do aquecimento em água
Estes testes serviram para identificar os seis tipos de plásticos conhecidos pelos códigos de identificação
1 - PET 2 - HDPE 3 - PVC 4 - LDPE 5 - PP 6 - PS
Classificação de polímeros
A produção de polímeros ocupa mais de 3/4 da indústria da Química Orgânica.
A indústria de plásticos em Portugal tem evoluído bastante. Na década de 90 a produção triplicou. Apesar de ser uma economia relativamente pequena, Portugal encontra-se entre os maiores fabricantes mundiais de moldes.
- Quanto à síntese, há polímeros produzidos por reacções de adição e outros por reacções de condensação. Essas reacções são polimerizações (a partir de monómeros).
- Quanto à origem os polímeros são naturais, artificiais ou semi-sintéticos e sintéticos;
- Quanto ao número de monómeros que os constituem, os polímeros são homopolímeros ou copolímeros (heteropolímeros);
- Em relação à sua degradação, existem alguns polímeros que são biodegradáveis, outros fotodegradáveis, outros são solúveis em água, ...
- De acordo com o comportamento mecânico, o material polimérico pode ser:
- Plástico - capaz de ser moldado em várias formas (filamentos, películas e outras); Os plásticos podem ser termoplásticos ou termofixos, de acordo com o efeito que o calor lhes provoca.
- Fibra -muito fino e alongado, na forma de filamentos. Constituído sobretudo por macromoléculas lineares. Fibras: naturais, artificiais, sintéticas.
Outros termos:
Resina - é uma substância amorfa ou uma mistura, de peso molecular intermédio ou alto, insolúvel em água mas solúvel em alguns solventes orgânicos e que, à temperatura ambiente, é sólida ou um líquido muito viscoso, que amolece gradualmente por aquecimento. Todas as resinas naturais são solúveis e fundíveis. Todos os polímeros sintéticos que possuem estas características também são conhecidos como resinas sintéticas.
Bioplástico - Plástico biodegradável (pode não ser obrigatoriamente biodegradável desde que tenha origem em matéria-prima renovável). Pode ser obtido a partir de origem natural ou de origem sintética...
Um universo de alto grau de conhecimento e de polímeros em construção, com muita fibra!
09/04/08
Oxidabilidade - índice de permanganato
Difusão do permanganato de potássio na água
O teor em sulfatos determina a necessidade de efectuar uma pré-oxidação no tratamento das águas superficiais ou subterrâneas destinadas à produção de água para consumo humano.
Pesquise e responda:
1. Refira 3 características da amostra que podem impedir a boa aplicação deste método de determinação da oxidabilidade.
08/04/08
Sulfatos na água
As suas principais origens são:
- Origem geológica (dissolução de gessos, oxidação de pirites, erosão de granito e basalto)
- Inquinação por dejectos;
- Utilização de fertilizantes (p.e. sulfato de amónio)
- Infiltração de águas do mar;
- Chuva ácida resultante da presença de óxidos de enxofre (dos combustíveis fósseis).
- Tratamento de águas (p.e. com o coagulante sulfato de alumínio); No entanto, esse coagulante pode ser removido por osmose inversa ou em resinas de permuta iónica.
Problemas associados à presença de elevado teor de sulfatos na água:
- Formação de inscrustrações em caldeiras e em permutadores de calor;
- Mau cheiro em tubagens de águas residuais - pela redução a ião sulfureto e formação de hidrogenossulfureto e ácido sulfídrico)
- Corrosão de tubagens de águas residuais - bactérias infectam as paredes das tubagens e, na presença de oxigénio transformam ácido sulfídrico em ácido sulfúrico;
O ião sulfato determina-se, por exemplo, através do método gravimétrico baseado na formação de um precipitado de sulfato de bário (devido à adição de cloreto de bário), o qual será digerido, filtrado, lavado, calcinado e pesado. É importante controlar o pH da amostra e ter em atenção várias interferências: matéria suspensa, silicatos, sulfatos, sulfitos, metais pesados, etc. A calcinação deve ocorrer numa mufla a 800 ºC.
Pesquise, discuta em grupo e responda:
1. Em que conhecimentos químicos (princípio) se baseia o método gravimétrico utilizado na determinação de sulfatos?
2.1. Indique duas interferências que podem proporcionar resultados mais elevados.
2.2. Indique duas interferências que podem proporcionar resultados mais baixos.
3. Qual o agente de precipitação utilizado? E qual o precipitado formado?
4. Determine a solubilidade do sulfato de bário a 25ºC.
5. Por que razões se adiciona polpa de papel de filtro*, se filtra em vácuo e se coloca o precipitado na mufla?
* O papel de filtro deve ser isento de cinzas.
02/04/08
Actividades laboratoriais - Dureza da água e cloretos
- o interesse da continuidade de análise do mesmo tipo (origem) de amostra de água;
- os apontamentos da sebenta e do manual:
 os materiais e os reagentes a utilizar;
os materiais e os reagentes a utilizar;
os procedimentos a seguir;
as observações a anotar assim como o registo de outros dados relevantes;
- a necessidade de efectuar cálculos para preparação das soluções;
- os cuidados a ter com os reagentes e materiais;
- a existência de soluções que deverão ser padronizadas e a preparação das respectivas soluções-padrão;
- as características da água a analisar e as interferências provocadas com o método de determinação;
- as cores apresentadas pelos indicadores (1, 2) a utilizar nas titulações;
- a realização de vários ensaios para cada determinação e usar os concordantes (média...) assim como a realização de ensaios em branco;
- o conhecimento e compreensão das reacções químicas intervenientes e das expressões de cálculo utilizadas na determinação dos parâmetros a obter;
Para além do habitual, o relatório deverá ter:
- uma introdução sobre o parâmetro a determinar e os conhecimentos de química envolvidos assim como os cuidados a ter com todos os reagentes utilizados;
- uma discussão dos resultados obtidos;
- os cuidados de preparação da actividade salientados neste post também deverão ser incluídos aquando da introdução e/ou da discussão.
Ainda há dúvidas sobre como se deve elaborar um relatório? Vá ao Brasil - MACKENZIE
E Que tal espreitar o blog de uma turma fantasquímica... » Dureza cálcica e dureza total da água.
/que inveja daqueles laboratórios/até cai aquela lágrima!...
07/03/08
Parâmetros da água
7ki -Oxidabilidade - índice de permanganato
7ki - Sulfatos - método gravimétrico
7ki - Dureza da água e cloretos
7ki - Cor, sabor, cheiro, turvação e condutividade
7ki - Qualidade da água - recolha e amostragem
Decreto-Lei: Qualidade da água destinada ao consumo humano - DL 306/2007 de 27 de Agosto
Boletim de resultados de análises - EMARP
Saponificação
Mas trata-se mesmo é de produzir sabão.
 Saponificação - reacção de hidrólise de ésteres de ácidos gordos em meio alcalino (soda cáustica - hidróxido de sódio, por exemplo).
Saponificação - reacção de hidrólise de ésteres de ácidos gordos em meio alcalino (soda cáustica - hidróxido de sódio, por exemplo).Para melhores resultados (sabão em barra) deve-se conseguir remover a glicerina. Mas atenção que a glicerina também serve para manter a humidade da pele ou humedecê-la.
Na fase final juntam-se os corantes e o perfume.
 Descubra a produção industrial de sabão e toda a explicação físico-química do processo »»» CATIM - Centro de Apoio Tecnológico à Indústria Metalomecânica
Descubra a produção industrial de sabão e toda a explicação físico-química do processo »»» CATIM - Centro de Apoio Tecnológico à Indústria MetalomecânicaDICAS E CURIOSIDADES - beleza.
25/02/08
Propriedades da água
7ki - Tensão superficial da água
Propriedades físicas da água
7ki & Biomoléculas
2 - Biomoléculas - proteínas
3 - Saponificação - sabão
No 2 - encontram-se muitos links para várias informações sobre todo o tipo de biomoléculas.
Home page
A explorar as primeiras amostras e parâmetros

1.1. E duas consequências.
2. O que é a condutividade eléctrica?
2.1. Em que unidades se pode apresentar?
2.2. Indique três factores que a influenciam o seu valor.
3. Obtenha valores paramétricos e outras indicações sobre cor, odor, sabor, turvação e condutividade no D.L. 306/2007.
22/02/08
Cor, sabor, cheiro, turvação e condutividade

São dois parâmetros subjectivos. Costumam ser avaliados por painéis de provadores.
Águas com teor em cloretos superior a 300 ppm são salgadas.
Águas com elevado teor de dióxido de carbono são picantes.
A determinação numérica do limiar de percepção do cheiro baseia-se na diluição sucessiva da água até que o odor deixe de ser perceptível.
O sabor e o cheiro surgem naturalmente, particularmente em fontes de água superficiais durante o Verão. Os compostos orgânicos que causam cheiro e sabor são removidos pelo tratamento de água (carbono activado ou ozono).
É a expressão numérica da capacidade de uma água conduzir a corrente eléctrica. Aumenta com a temperatura. Aumenta muito com a presença de impurezas predominantemente iónicas. A medição é feita através de um condutivímetro. Permite uma avaliação do grau de mineralização da água e contribui para controlo do tratamento.
Valores a 18ºC: águas doces, de 100 a 2000 microS/cm
água do mar 45000 microS/cm
19/02/08
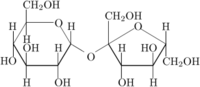
Muito açúcar!
Biomoléculas - proteínas
 As proteínas são polímeros naturais. Um polímero é uma molécula muito grande formada pela ligação repetida de moléculas mais pequenas, os monómeros.
As proteínas são polímeros naturais. Um polímero é uma molécula muito grande formada pela ligação repetida de moléculas mais pequenas, os monómeros.As proteínas são polímeros naturais (copolímeros) de alfa-aminoácidos condensados, formando cadeias polipeptídicas muito longas que se dispõem com formas características pelo espaço.
Existem cerca de 10 000 proteínas do corpo humano. Podemos destacar a fundamental importância das proteínas por serem as constituintes de todas as células humanas e também por terem um carácter estrutural. As proteínas estão presentes em todos os processos biológicos.
Em química, um aminoácido é uma molécula que contém simultaneamente grupos funcionais amina e carboxilo. Os aminoácidos, por uma reacção de condensação, unem-se em cadeia através de ligações peptídicas e formam péptidos (ou peptídeos).
Os aminoácidos, por uma reacção de condensação, unem-se em cadeia através de ligações peptídicas e formam péptidos (ou peptídeos).
As cadeias que contêm entre 2 e 20 aminoácidos são os oligopéptidos. Com mais de 20 aminoácidos já são polipéptidos (existem polipéptidos com mais de 100 aminoácidos). Então, as proteínas são polipéptidos.
Já agora, pense nisto:
"Os prótidos podem ser aminoácidos, peptídeos ou proteínas".
Será que esta ideia tem alguma lógica ou não?
- As proteínas são constituídas a partir dos 20 alfa-aminoácidos principais.*
- As proteínas são compostos quaternários contituídos pelos elementos C, H, O e N. Em alguns casos também contêm enxofre (S) ou até outros elementos.
- Os aminoácidos têm constantes de acidez e de basicidade muito baixas e não se dissolvem em solventes não polares.
- Os aminoácidos são solúveis na água.
Proteínas na Cozinha? Aqui. E também Ciência Viva nas Farófias!
11/02/08
Algumas propriedades da água - tensão superficial
A tensão superficial resulta do desequilíbrio das forças intermoleculares estabelecidas pelas moléculas na superfície do líquido. Pode ser entendida como a quantidade de energia necessária para reduzir ao mínimo a área superficial do fluido. Ou como a energia necessária para criar uma área unitária de superfície; ou ainda, a força tangencial que a superfície exerce por unidade de comprimento.
A tensão superficial da água é cerca de 0,075 N/m. A do álcool é 0,024 N/m. É mais difícil formar gotas de álcool que de água, nas mesmas condições.
A tensão superficial da água é responsável por:
- fios de água pararelos ficarem unidos após lhes tocarmos em conjunto;
- alguns insectos passearem sobre a água;
- as bolas de sabão terem um formato esférico;
- as gotas de água grandes serem ovais e as mais pequenas circulares;
- se notar o efeito de um detergente na água (quebra as ligações intermoleculares e faz diminuir a tensão superficial); Assim também se favorece a remoção das gorduras pelo detergente.
Observações interessantes: A água espalha-se facilmente numa placa de vidro limpa; numa proveta nota-se que se adapta bem às paredes e fica sempre com um nível mais elevado junto às paredes do que no centro do menisco.
22/01/08
Qualidade das águas - recolha e amostragem
2 - Indicações de recolha de água (de consumo humano) para análise, da empresa Águas do Cávado. Distinção de método em função do tipo de análise a realizar.

Métodos de recolha, armazenamento e transporte de vários tipos de águas, do Instituto do Ambiente. Interesse especial nos diapositivos 2-11, 14-24, 33 -37, 41-44, 45-49, 53-64, 65-73, transporte - 74, 75, fontes de erro - 79-83 85-86 - conclusões sobre amostragem
Mais perguntas frequentes sobre a água: abastecimento e qualidade. FAQs.
EPAL - Empresa Portuguesa das Águas Livres, SA
1. Efectue a simulação para o consumo de água da sua habitação (em "Clientes").
2. Encontre a lista de Materiais de Construção Aprovados na EPAL e indique 3 materiais usados em tubagens (em "Laboratório Central - Qualidade da Água").
3. Indique as diversas origens da água da EPAL.
4. Indique os tratamentos que a água superficial sofre na ETA da Asseiceira.
5. Indique 5 municípios que são abastecidos em alta pela EPAL.
6. Indique o significado de "dureza da água".
7. Comente "Quando a água está branca é imprópria para consumo".
8. Indique a técnica utilizada na determinação de bromatos e de brometos. (Indique também as fórmulas desses iões.)
9. Indique as fórmulas de estrutura de 3 compostos orgânicos que constem dos parâmetros possíveis de determinar numa análise de água.
10. Qual é a norma segundo a qual se encontra certificado o SGA - sistema de gestão ambiental da EPAL?
11. Qual é a norma de acordo com a qual se encontra acreditado o Laboratório da Asseiceira?
12. Indique duas metas do SGA para 2007, em relação à qualidade da água. (Refira IVPs.**)
"Hiperligue-se" com o EPAL-Júnior e o seu ciclo da água!
Extra - bónus!
13. Como se chama a publicação - Jornal da EPAL?
14. O que é o "H2Olha"?
15. Quais são os 9 temas que têm objectivos definidos (no SGA) para 2007?
16. Quanta água perdeu o Zé das Máquinas na tentativa de ajudar o João?
* em "Utilitários" encontra o mapa do site, para facilitar a sua pesquisa...
** Incumprimentos de Valores Paramétricos.
15/01/08
Qualidade da água para consumo humano
Analise o documento (no site do IRAR) e responda:
1. O que se entende por água destinada ao consumo humano?
E por:
1.1. água salubre e limpa 1.2.fontes individuais 1.3. substância perigosa 1.4. valor paramétrico
2. Como é que pode concluir que uma água é salubre e limpa?
3. Este D.L. aplica-se às águas minerais? Porquê?
4. Indique uma situação em que, apesar da água ser destinada ao consumo humano, pode ser concedida isenção de aplicação das normas deste D.L.
5. A que entidades compete assegurar que a água satisfaz as exigências de qualidade?
6. Que entidade pode fixar valores aplicáveis a outros parâmetros adicionais?
7. Indique dois tipos de pontos em que se efectua a verificação dos valores paramétricos.
8. Indique duas medidas que a autoridade competente (qual é?) pode tomar em caso de não cumprimento dos valores paramétricos.
9. Refira alguns elementos do programa mínimo de controlo de qualidade da água.
10. Que acções de vigilância sanitária competem às autoridades de saúde?
11. O que deve fazer a entidade gestora quando se verifica um incumprimento dos valores paramétricos?
12. A quem compete as acções de inspecção relativas à qualidade da água?
12.1. E que entidades deve alertar sobre as eventuais irregularidades?
13. Em que artigo e pontos do D.L. se baseia para permitir, em alguns casos de abastecimento público, o não cumprimento de valores paramétricos.
14. Indique o nome do relatório técnico anual que conhece e que se enquadra no ponto 1. do art. 16º.
15. A que entidade compete a instrução de processos de contra-ordenação referidos no art. 22º?
15.1. O que entende por "a negligência é punível"?
16. Indique os 3 tipos de parâmetros a analisar numa água.
17. O que é o controlo de rotina?
17.1. E o controlo de inspecção?
18. Quantas análises por ano devem ser feitas (no mínimo) ao parâmetro ferro? Justifique.
19. Indique dois parâmetros para os quais não se especifica qualquer método de análise.
Indicações num laboratório de análise de águas. Aqui.
D.L. 243/2001 no D.R. (com quadros e anexos)
09/01/08
PEAASAR II 2007-2013
- a sua exequibilidade nos calendários previstos e os meios disponíveis;
- os modelos de gestão e de financiamento adequados à resolução da problemática dos sistemas em “baixa” e à sua articulação com os sistemas em “alta”;
- as bases de uma política tarifária a nível nacional;
- as fontes de financiamento, o enquadramento financeiro das acções a desenvolver e as condições de acesso aos financiamentos;
- a clarificação do papel dos intervenientes públicos e privados no processo;
- o alargamento do leque de alternativas de infra-estruturação e gestão e o reforço e alargamento dos poderes regulatórios.
Apresentação pública do PEAASAR II (em Março de 2006)
07/01/08
Em exploração - IRAR
1. No seu estatuto, identifique qual o objecto do IRAR e 3 das suas atribuições.
2. Identifique as duas missões em que se divide o âmbito de actuação do IRAR.
3. Onde e quando se irá organizar o 9º Congresso da Água? Qual é a entidade organizadora?
4. Qual é a lei (mais actual) que é conhecida como Lei da Água?
5. Na apresentação do "sector das águas":
5.1. O que compreende (está incluido no) o sector de serviços de águas?
5.2. Indique um nível de cobertura cuja meta tenha sido alcançada (ou ficado muito perto de atingir) no PEAASAR 2000-2006.
5.3. Indique uma meta que tenha ficado longe de ser alcançada no PEAASAR 2000-2006.
5.5. Quais são as 6 etapas da cadeia de valor do sub-sector "águas"?
6. Identifique as entidades gestoras no concelho da Chamusca. Descubra em que sub-sector(es) se enquadra cada uma delas.
7. Indique duas entidades gestoras responsáveis pelo sistema de distribuição de água em alta.
8. Uma questão que muitas vezes se coloca é a da avaliação da qualidade da água que consumimos.
8.1. Como é avaliada a qualidade da água pelo IRAR?
8.2. Onde se podem consultar os resultados das análises sobre a qualidade da água? Encontre alguns desses resultados no site.
9. Em caso de escassez de água, existe alguma priorioridade de utilização? Se sim, qual?
10. Se proceder a uma descarga de águas residuais está a proceder a uma ilegalidade. Justifique com base na legislação.
Em exploração IRAR -2
11. O que é o RASARP?
11.1. Qual foi a entidade gestora, em alta, que apresentou, em 2006, maior % de água não facturada?
11.2. E para as entidades gestoras em baixa, entre que valores variou essa %?
12. Para a entidade gestora Águas do Norte Alentejano, S.A. (2006), indique:
12.1. o preço médio do seu serviço;
12.2. a % de análises de água efectuadas das previstas na legislação;
12.3. a % de análises de água que respeitou os valores definidos pela legislação;
12.4. a capacidade de reserva da água tratada;
12.5. o nº de avarias em condutas por cada 100 km;
12.6. a ineficiência na utilização dos recursos hídricos.
13. Efectue uma listagem dos parâmetros medidos numa análise de água.
14. Em 2006, que entidades gestoras em alta apresentaram maiores problemas com a qualidade da água? (Indique apenas 5 dessas entidades).
03/01/08
Poluição das águas subterrâneas
 Uma água está poluída quando a sua composição foi alterada de tal maneira que a torna imprópria para um determinado fim.
Uma água está poluída quando a sua composição foi alterada de tal maneira que a torna imprópria para um determinado fim.As causas fundamentais da poluição das águas subterrâneas ocasionada pela actividade humana podem agrupar-se em quatro grupos dependendo da actividade humana que as originou:
1. Poluição urbana e doméstica;
2. Poluição agrícola;
3. Poluição industrial;
4. Contaminação induzida por bombeamento (associada à intrusão salina).
Ver mais em... geociências
Digam lá outra vez...
Aventuras no Lab5
Química e Ambiente
A ciência Química e as Tecnologias do Ambiente.

Imagens verdes - "cidadeverde.com"